一氧化碳还原氧化铁实验
探索工业炼铁的化学原理 🧪
实验控制
实验进度
步骤 1/7
当前步骤
检查装置气密性
慢
快
当前速度: 1.0x
实验步骤
实验装置
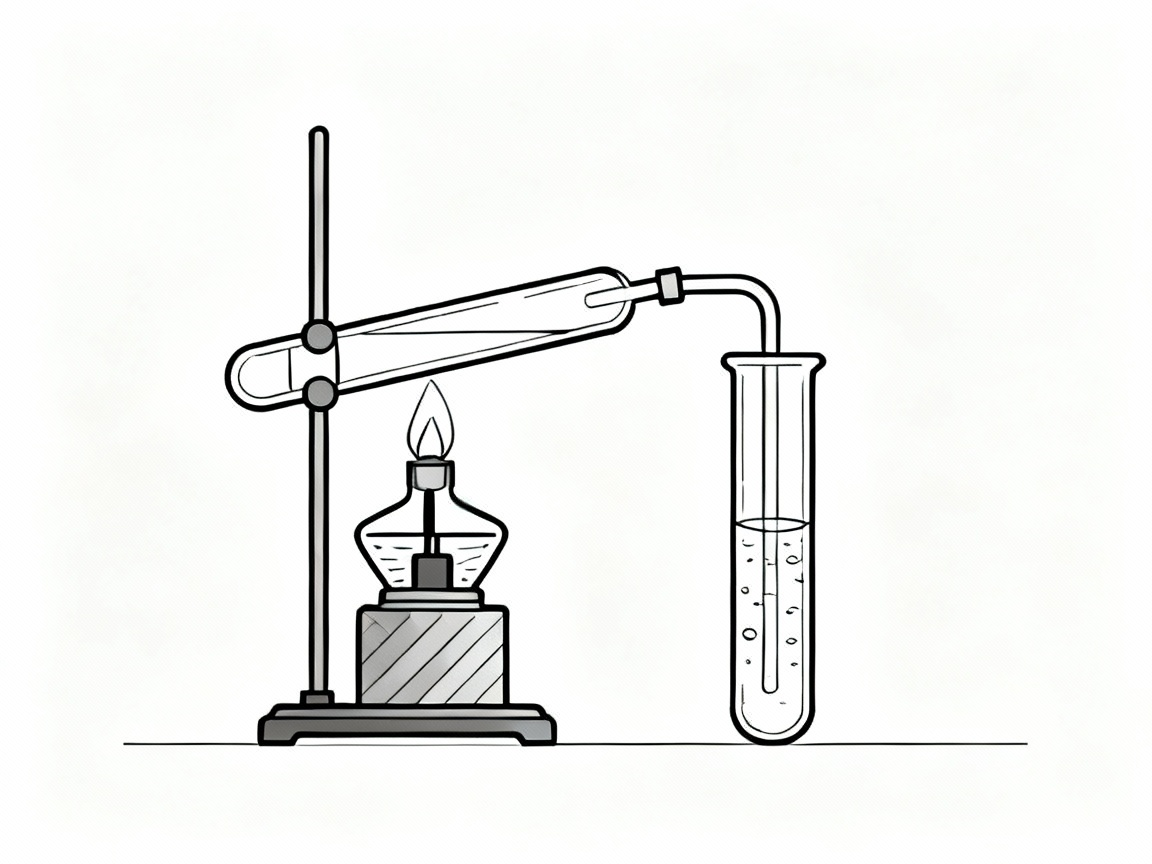
实验现象
🔴
玻璃管内
红棕色粉末逐渐变成黑色
 →
→

💧
试管内
澄清石灰水变浑浊
证明生成了CO₂
🔥
尾气处理
尾气燃烧产生蓝色火焰
防止CO污染空气
化学原理
主反应(高温条件)
3CO + Fe₂O₃ 高温→ 2Fe + 3CO₂
• CO作还原剂,具有还原性
• Fe₂O₃被还原,失去氧元素
检验CO₂生成
Ca(OH)₂ + CO₂ → CaCO₃↓ + H₂O
• 澄清石灰水变浑浊,证明有CO₂生成
尾气处理
2CO + O₂ 点燃→ 2CO₂
• 防止有毒CO排放到空气中
安全注意事项
⚠️
实验前:先通CO,再加热
目的:排尽玻璃管内的空气,防止加热时CO与空气混合发生爆炸
⚠️
实验后:先停止加热,继续通CO至冷却
目的:防止高温下的铁被空气中的氧气再次氧化,同时防止石灰水倒吸
☠️
尾气处理:必须点燃或收集
CO有毒,不能直接排放到空气中,必须燃烧转化为CO₂或用气球收集
💡
操作口诀
"一氧化碳早出晚归,酒精喷灯迟到早退"
意思:CO先通入后停止,加热后开始先停止